Universitätsklinik für Neurochirurgie
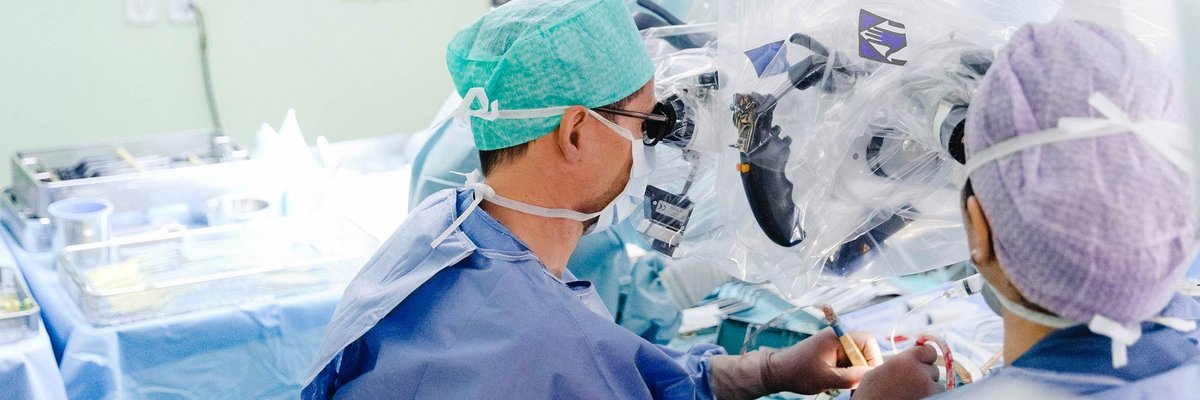
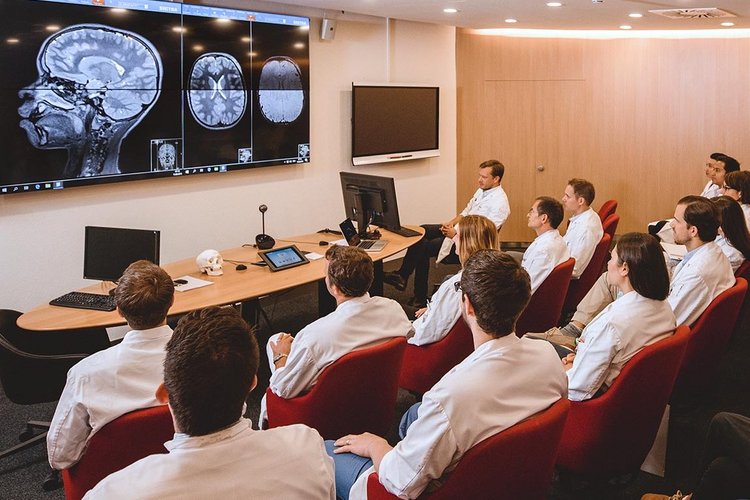
Die Universitätsklinik für Neurochirurgie am Inselspital ist eine international renommierte Klinik für die operative Behandlung von Erkrankungen des Gehirns und der Wirbelsäule. Hier bieten wir Ihnen einen umfassenden Einblick in unsere Klinik und erleichtern den Kontakt zu uns. Herzlich willkommen!
Zweitmeinung
Sind Sie unsicher? Dann holen Sie sich von unseren Spezialisten eine fundierte Zweitmeinung ein.
Internationale Patienten
Unseren internationalen Patienten steht unser Insel International Center hilfreich zur Seite.
Jobs & Karriere
Suchen Sie eine neue spannende Herausforderung im Bereich der Neurochirurgie?