Le fiber tracking est une technique d'analyse spécifique des images IRM qui permet de visualiser les principales voies de fibres nerveuses du cerveau. Ces voies relient différentes régions cérébrales et sont notamment responsables du mouvement, du langage ou de la vision. Avant une intervention neurochirurgicale, le fiber tracking aide à cartographier le tracé exact de ces structures sensibles. Cela permet de planifier les interventions avec plus de précision et de mieux protéger les fonctions cérébrales essentielles.
Qu’est-ce que le fiber tracking ?
Le fiber tracking est une technique d'analyse spécifique des images IRM du cerveau. Cette méthode permet de visualiser les faisceaux de fibres nerveuses. Ces faisceaux relient différentes zones du cerveau entre elles et sont notamment responsables du mouvement, du langage ou de la vision.
Dans certaines pathologies, comme les tumeurs cérébrales, ces connexions importantes peuvent passer à proximité de la région touchée. Le « fiber tracking » nous aide à retracer le tracé exact de ces faisceaux nerveux.
Comment fonctionne le fiber tracking ?
Le fiber tracking repose sur une technique d'IRM spécifique, appelée imagerie par diffusion. Celle-ci consiste à mesurer le mouvement des molécules d'eau dans le tissu cérébral. Dans les fibres nerveuses, l'eau se déplace principalement dans le sens des fibres. Cette propriété permet de déterminer mathématiquement le tracé des faisceaux de fibres et de le rendre visible.
À l'aide d'un logiciel spécialisé, ces données permettent de créer des représentations tridimensionnelles des voies nerveuses.
Limites de la méthode
Le fiber tracking représente des faisceaux de fibres nerveuses, et non des nerfs individuels, car la résolution de l'imagerie par résonance magnétique sur laquelle il s'appuie est limitée. De plus, la représentation repose sur des modèles mathématiques et peut être influencée par divers facteurs.
Malgré les techniques d'imagerie modernes telles que le fiber tracking haute définition, des ruptures inattendues des fibres reconstruites continuent de se produire aux points de croisement et dans les zones où les fibres changent de direction dans un espace restreint. Sélectionner les fibres pertinentes, vérifier leur plausibilité et les préparer en vue de leur utilisation pour la planification chirurgicale est une tâche exigeante qui nécessite l'intervention d'un spécialiste.
Malgré ces limites, cette méthode fournit des informations supplémentaires importantes et constitue aujourd'hui un outil précieux dans la planification moderne des interventions neurochirurgicales.
Comment le fiber tracking est-il utilisé à l'Inselspital ?
Cette technique est principalement utilisée pour la planification des interventions neurochirurgicales.
Lorsqu'une tumeur cérébrale ou une autre lésion se trouve à proximité de voies nerveuses importantes, il est essentiel de connaître leur trajet. Le fiber tracking aide nos neurochirurgiens à :
- identifier les voies nerveuses importantes
- planifier la meilleure voie d'abord chirurgicale possible
- réduire le risque de troubles fonctionnels
Les informations obtenues peuvent être intégrées à la planification chirurgicale et à la navigation peropératoire.
L'objectif est d'assurer une ablation radicale, même des tumeurs situées dans des zones fonctionnelles importantes du cerveau. En association avec les techniques de neurophysiologie peropératoire, nous parvenons ainsi à offrir à nos patients une radicalité maximale avec une invasivité minimale et une préservation importante des fonctions.
Afin de rendre les interventions chirurgicales encore plus sûres pour les patients à l'avenir, la recherche et le développement de techniques innovantes telles que le fiber tracking constituent chez nous, à l'Inselspital, un axe de recherche à part entière.
Le fiber tracking dans l'application clinique
- Planification des fiber tracks
Lorsqu'une opération doit avoir lieu à l'aide du fiber tracking, les séquences DTI spécialement nécessaires ainsi que les séquences d'images pondérées en T2 sont créées et assemblées au préalable dans une IRM de 3 Tesla. Les artefacts (artefacts de courant d'Eddy et artefacts de mouvement) sont automatiquement éliminés au moyen d'un algorithme automatique. Pour calculer les faisceaux de fibres souhaités, une région d'intérêt (ROI) est placée sur les points de repère anatomiques pertinents dans l'imagerie IRM pondérée en T2. En outre, on choisit les paramètres pour l'anisotropie fractionnelle et la longueur des faisceaux de fibres.
Par exemple, pour calculer la trajectoire pyramidale, les régions d'intérêt sont tracées le long des repères anatomiques d'imagerie de la trajectoire pyramidale sur les images pondérées en T2 : Gyrus précentral, Capsula interna ainsi que des parties du pédoncule cérébral. En choisissant correctement les paramètres de réglage, on obtient un faisceau de fibres homogène qui représente le tracé de la voie pyramidale.
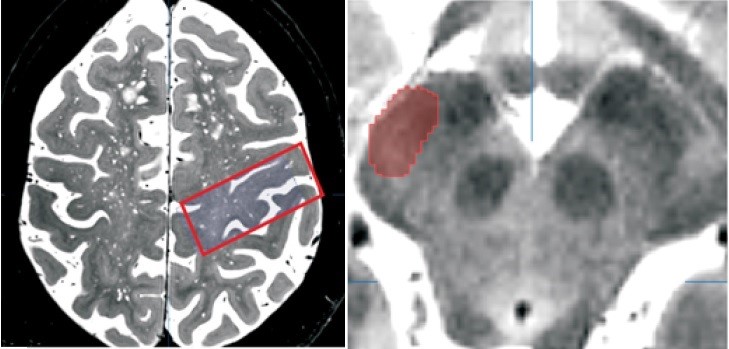
Zones d'intérêt (ROI). Sur les images IRM pondérées en T2, les régions d'intérêt (ROI) sont marquées pour le calcul du tractus corticospinal. Le tractus corticospinal prend naissance dans le gyrus précentral (image de gauche) et traverse le crus cerebri (image de droite) pour rejoindre la moelle épinière. Bild: Nowacki et. al. 2018, JNS - Le fiber tracking en chirurgie tumorale
Si une tumeur se trouve à proximité d'un faisceau de fibres important, le fiber tracking est nécessaire pour garantir une sécurité maximale au patient. Souvent, les limites entre le tissu cérébral sain et le tissu tumoral ne peuvent pas être clairement délimitées. Le tracé exact des faisceaux de fibres par rapport à la tumeur fournit alors au chirurgien des informations supplémentaires importantes qui ne sont pas visibles de cette manière avec les yeux.
En combinaison avec d'autres techniques telles que le neuromonitoring peropératoire, le chirurgien dispose de plusieurs possibilités pour s'assurer qu'aucune structure critique n'est endommagée pendant l'opération. En particulier, les connexions fibreuses nécessaires aux fonctions humaines de base telles que la parole, la vision et le mouvement sont protégées à grands frais contre les dommages involontaires pendant l'opération de la tumeur.
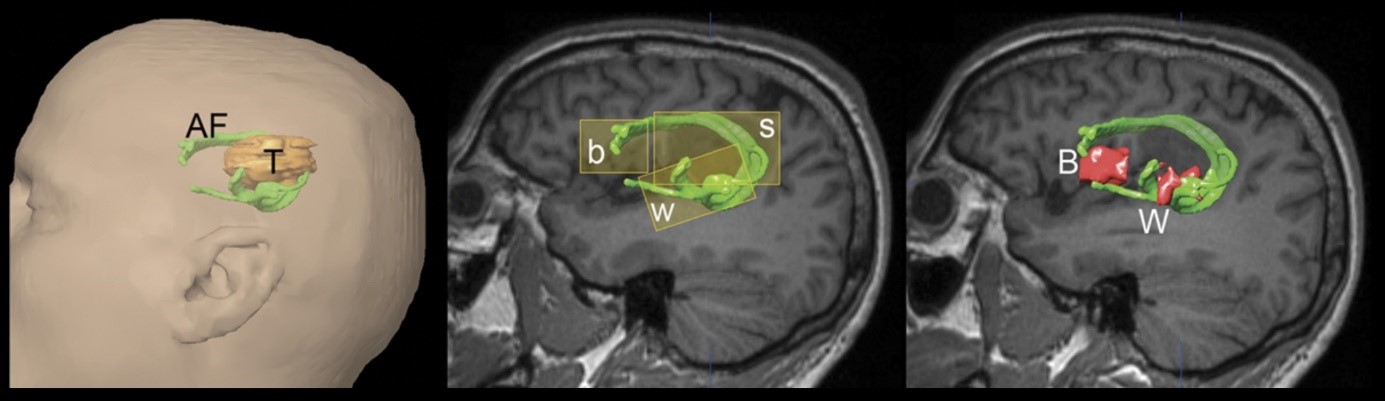
Chirurgie tumorale. (À gauche) La tumeur à exciser (T) se trouve à proximité immédiate du faisceau arqué (AF). L'image du milieu montre les « voxels d'intérêt » (VOI) qui ont été utilisés pour calculer le faisceau de fibres. À droite, on voit le tracé du faisceau arqué avec le centre de Broca (B) et l'aire de Wernicke (W) situés respectivement aux extrémités du faisceau de fibres. Bild: Stieglitz et. al. 2012, Neurosurgery 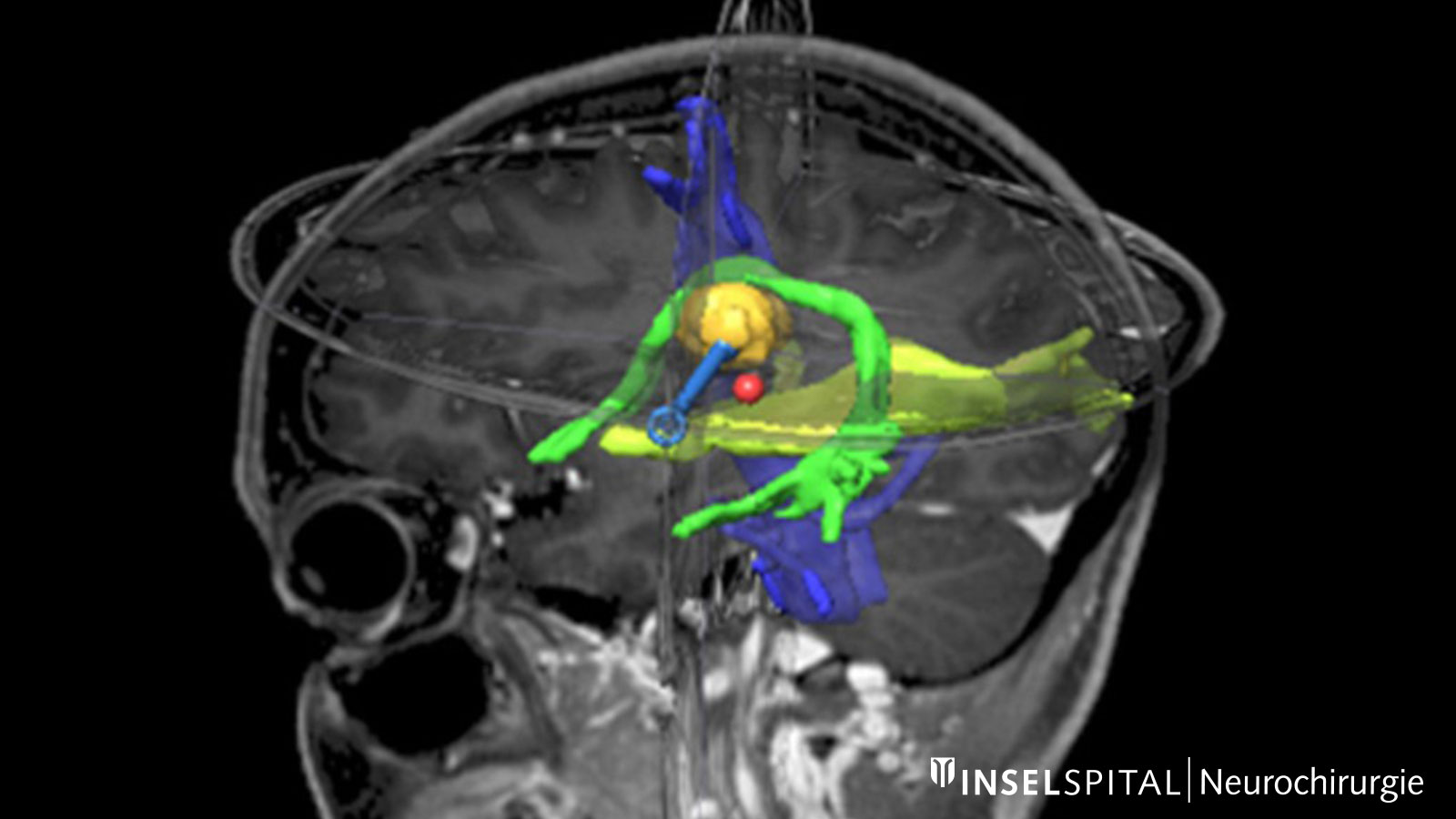
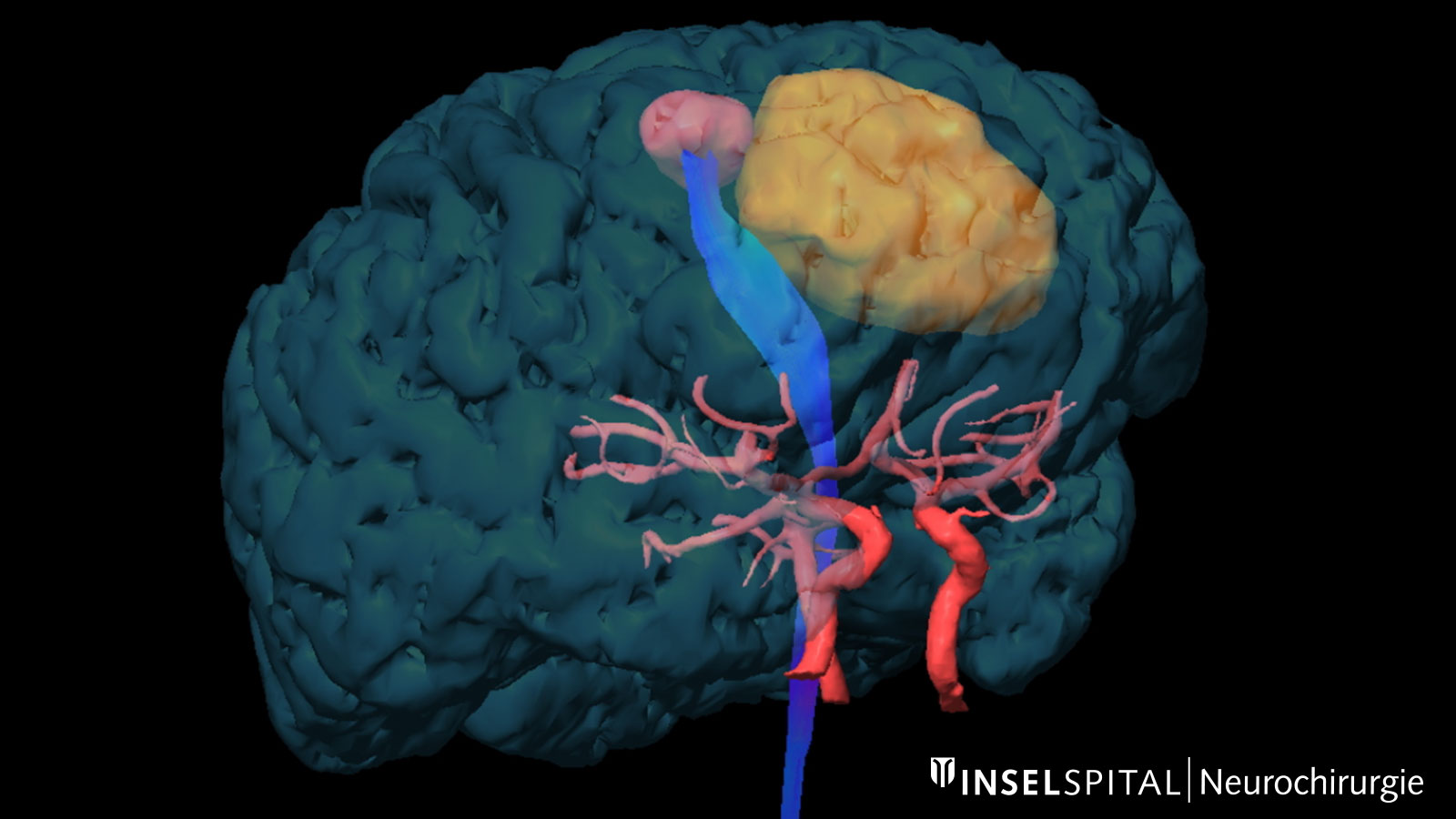
Zones névralgiques. Cette illustration montre une tumeur (orange) située au milieu de zones fonctionnellement importantes : le tractus corticospinal (bleu), le tractus optique (jaune) et le faisceau arqué (vert) Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 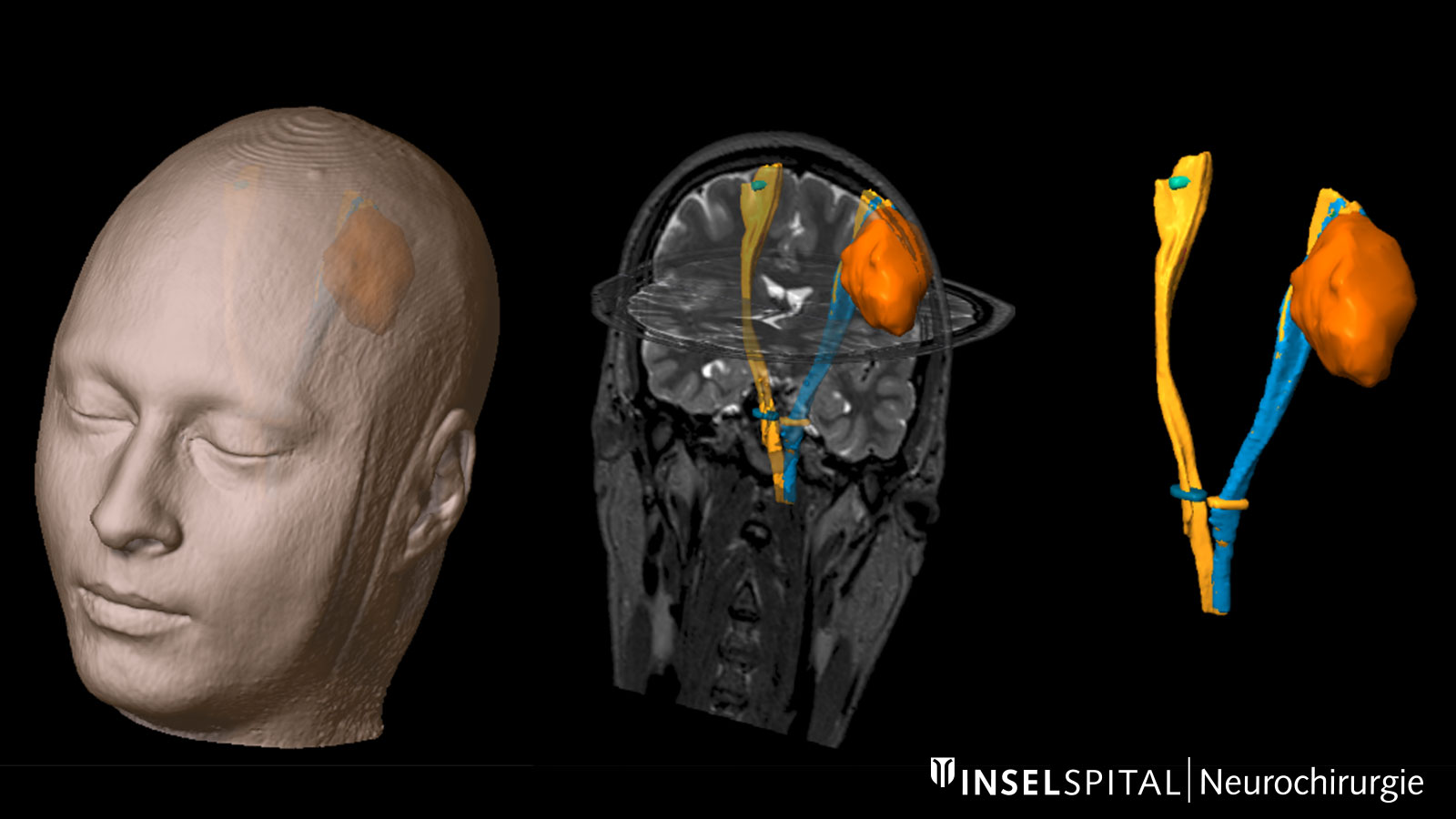
Trajet corticospinal. Le trajet corticospinal (en jaune et bleu) est représenté ici comme une voie de transmission de la fonction motrice en relation avec une tumeur (en orange). Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 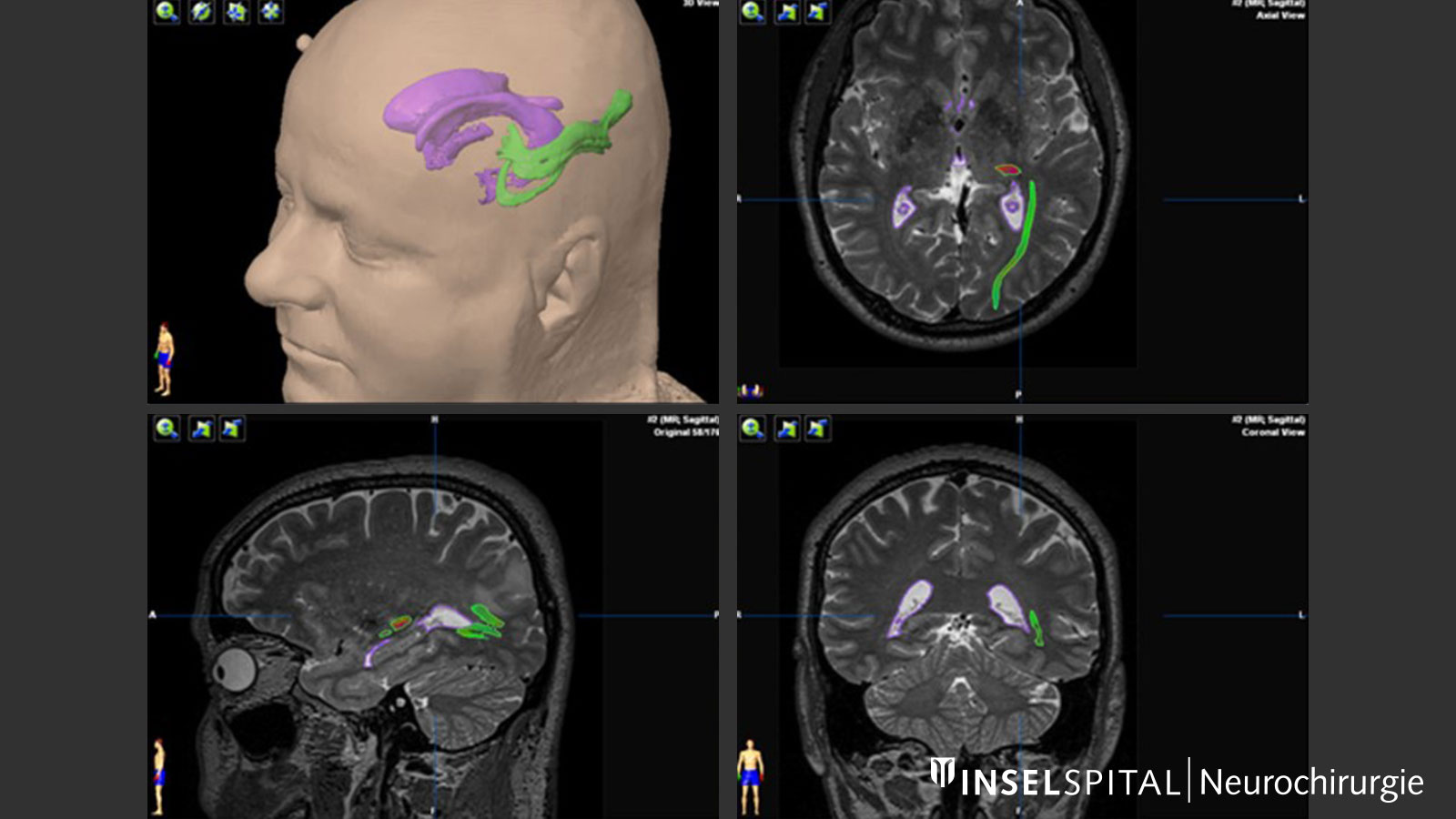
Voie optique. Cette illustration montre comment la voie optique (tractus opticus, en vert) contourne le système ventriculaire (en violet). Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 - Fiber tracking pour la stimulation cérébrale profonde
Fiber tracking dans le tremblement essentiel
Dans le cas du tremblement essentiel, nous utilisons le fiber tracking pour visualiser le tractus dentatorubothalamique (DRTT) afin de planifier la stimulation des voies fonctionnelles. Le fiber tracking complète ici la planification traditionnelle, purement anatomique. La voie dento-sous-thalamique (DRTT) se trouve dans l'aire sous-thalamique postérieure (PSA) et constitue l'un des points cibles de la stimulation cérébrale profonde (SCP) pour le traitement du tremblement essentiel *. La localisation exacte est indispensable lors de la planification de l'opération afin de permettre une stimulation précise du tractus. Grâce au fiber tracking, il est possible de visualiser le tractus et de déterminer de manière optimale les points cibles pour l'implantation des électrodes SCP.

Stimulation cérébrale profonde dans le traitement de la maladie de Parkinson. L'image de gauche montre la visualisation du tractus dento-rubro-thalamique afin de planifier l'implantation correcte des électrodes (en rouge) dans le cadre d'une stimulation cérébrale profonde. L'image de droite indique la localisation exacte de la cible, afin que la stimulation puisse avoir lieu juste à côté du DRTT. Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 Fibre tracking en cas de dépression
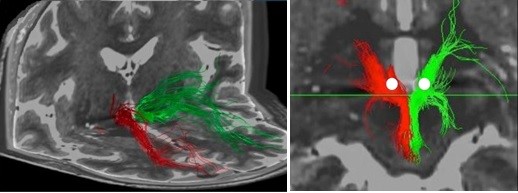
Stimulation cérébrale profonde dans le traitement de la dépression. L'image de gauche présente une reconstruction en 3D des faisceaux médians antérieurs droit (en rouge) et gauche (en vert) du cerveau. Sur l'image de droite, les points cibles pour le placement des électrodes avant la stimulation cérébrale profonde sont indiqués par des points blancs. Bild: Fenoy et. al. 2016, J Affect Disord Un autre domaine d'application clinique pour le fiber tracking à l'Inselspital est la thérapie par stimulation cérébrale profonde (SCP) dans les cas graves de dépression qui ne répondent pas à la thérapie habituelle. Des études médicales ont montré que la stimulation de la partie superolatérale du faisceau cérébral antérieur médian avait un effet thérapeutique positif dans les dépressions réfractaires *. Afin d'identifier correctement le faisceau de fibres et de déterminer les coordonnées de la cible pour la SCP, il est nécessaire de procéder à un suivi des fibres avant l'intervention.
-
Nowacki A, Debove I, Rossi F, Schlaeppi J, Petermann K, Wiest R, Schüpbach M, Pollo C. Targeting the posterior subthalamic area for essential tremor: proposal for MRI-based anatomical landmarks. Journal of Neurosurgery. 2018;1-8.
-
Fenoy AJ, Schulz P, Selvaraj S, Burrows C, Spiker D, Cao B, et. al. Deep brain stimulation of the medial forebrain bundle: Distinctive responses in resistant depression. J Affect Disord. Oktober 2016;203:143–51.
