Fiber Tracking ist eine spezielle Auswertung von MRI-Bildern, mit der wichtige Nervenfaserbahnen im Gehirn sichtbar gemacht werden können. Diese Bahnen verbinden verschiedene Hirnregionen und sind unter anderem für Bewegung, Sprache oder Sehen verantwortlich. Vor neurochirurgischen Operationen hilft Fiber Tracking dabei, den genauen Verlauf dieser empfindlichen Strukturen darzustellen. Dadurch können Eingriffe präziser geplant werden und wichtige Funktionen des Gehirns besser geschützt werden.
Was genau ist Fiber Tracking?
Fiber Tracking ist eine spezielle Auswertung von MRI-Bildern des Gehirns. Mit dieser Methode können wichtige Nervenfaserbahnen sichtbar gemacht werden. Diese Bahnen verbinden verschiedene Bereiche des Gehirns miteinander und sind zum Beispiel für Bewegung, Sprache oder Sehen verantwortlich.
Bei bestimmten Erkrankungen, etwa bei Hirntumoren, können diese wichtigen Verbindungen in der Nähe der betroffenen Region verlaufen. Fiber Tracking hilft uns, den genauen Verlauf dieser Nervenbahnen darzustellen.
Wie funktioniert Fiber Tracking?
Fiber Tracking basiert auf einer speziellen MRI-Technik, der sogenannten Diffusionsbildgebung. Dabei wird gemessen, wie sich Wassermoleküle im Gehirngewebe bewegen. In den Nervenfasern bewegt sich Wasser bevorzugt entlang der Faserrichtung. Diese Eigenschaft ermöglicht es, den Verlauf von Faserbahnen rechnerisch zu bestimmen und sichtbar zu machen.
Mit Hilfe spezieller Software werden aus diesen Daten dreidimensionale Darstellungen der Nervenbahnen erstellt.
Grenzen der Methode
Fiber Tracking stellt Bündel von Nervenfasern dar, nicht einzelne Nerven, denn die Auflösung der zugrundeliegenden Magnetresonanztomografie ist begrenzt. Ausserdem basiert die Darstellung auf mathematischen Modellen und kann durch verschiedene Faktoren beeinflusst werden.
Trotz moderner bildgebender Verfahren wie dem High Definition Fiber Tracking ergeben sich auch weiterhin unerwartete Abbrüche der rekonstruierten Fasern an Kreuzungsstellen und im Bereich von Fasern, die auf engem Raum die Verlaufsrichtung ändern. Die relevanten Fasern herauszusuchen, auf ihre Plausibilität zu prüfen und sie für die Verwendung zur Operationsplanung vorzubereiten, ist anspruchsvoll und erfordert einen Spezialisten.
Trotz dieser Einschränkungen liefert das Verfahren wichtige zusätzliche Informationen und ist heute ein wertvolles Instrument in der modernen neurochirurgischen Operationsplanung.
Wie wird Fiber Tracking am Inselspital eingesetzt?
Das Verfahren wird vor allem zur Planung neurochirurgischer Operationen eingesetzt.
Wenn ein Hirntumor oder eine andere Veränderung nahe an wichtigen Nervenbahnen liegt, ist es entscheidend zu wissen, wo diese verlaufen. Fiber Tracking hilft unseren Neurochirurginnen und Neurochirurgen:
- wichtige Nervenbahnen zu identifizieren
- den bestmöglichen Operationszugang zu planen
- das Risiko für Funktionsstörungen zu reduzieren
Die gewonnenen Informationen können in die Operationsplanung und Navigation während der Operation integriert werden.
Das Ziel ist dabei eine radikale Entfernung auch von Tumoren in wichtigen funktionellen Arealen des Gehirns. Zusammen mit den Verfahren der intraoperativen Neurophysiologie erreichen wir so für unsere Patienten eine maximale Radikalität bei minimaler Invasivität und wichtigem Funktionserhalt.
Damit Operationen für den Patienten zukünftig noch sicherer werden, bilden die Erforschung und Weiterentwicklung von innovativen Techniken wie das Fiber Tracking bei uns am Inselspital einen eigenen Forschungsschwerpunkt.
Fiber Tracking in der klinischen Anwendung
- Planung der Fiber Tracks
Wenn eine Operation mit Hilfe von Fiber Tracking stattfinden soll, werden im Vorfeld dafür die speziell benötigten DTI-Sequenzen sowie T2-gewichtete Bildsequenzen in einer 3-Tesla-Magnetresonanztomografie erstellt und zusammengefügt. Mittels eines automatischen Algorithmus werden Artefakte (Eddy-Current-Artefakte und Bewegungsartefakte) automatisch eliminiert. Zur Berechnung der gewünschten Faserbündel wird nun eine sogenannte Region of Interests (ROI) über die relevanten anatomischen Landmarken in der T2-gewichteten MRI-Bildgebung gelegt. Ausserdem wählt man die Parameter für die fraktionale Anisotropie und Faserbündellänge aus.
Um beispielsweise die Pyramidenbahn zu berechnen werden die Regions of Interest entlang den bildgebenden anatomischen Landmarken der Pyramidenbahn auf den T2-gewichteten Bildern eingezeichnet: Gyrus precentralis, Capsula interna sowie Teile des Pedunculus cerebri. Mit den richtig gewählten Einstellungsparametern erhält man ein homogenes Faserbündel, welche den Verlauf der Pyramidenbahn darstellt.
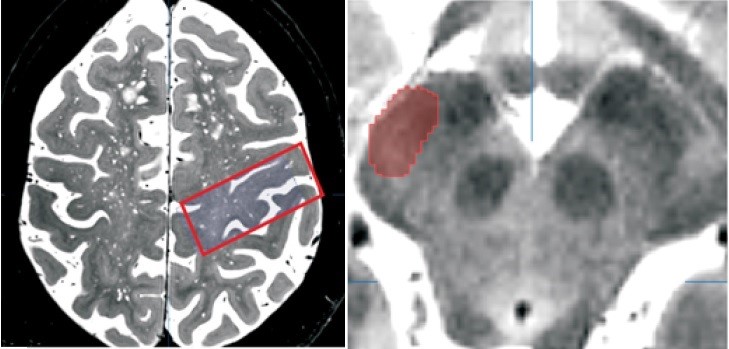
Regions of Interest (ROI). In T2-gewichteten MRI-Bildern werden die Regions of Interest (ROI) zur Berechnung der Pyramidenbahn markiert. Die Pyramidenbahn (Tractus corticospinalis) nimmt ihren Ursprung im Gyrus precentralis (linkes Bild) und verläuft über das Crus cerebri (rechtes Bild) in das Rückenmark. Bild: Nowacki et. al. 2018, JNS - Fiber Tracking in der Tumorchirurgie
Sollte ein Tumor in der Nähe eines wichtigen Faserbündels liegen, ist ein Fiber Tracking notwendig, um maximale Patientensicherheit zu gewährleisten. Oftmals sind die Grenzen zwischen gesundem Gehirngewebe und Tumorgewebe nicht eindeutig abzugrenzen. Der genaue Verlauf der Faserbündel in Relation zum Tumor liefert dem Chirurgen dann wichtige Zusatzinformationen, die mit den Augen so nicht sichtbar sind.
Zusammen mit anderen Techniken wie beispielsweise dem intraoperativen Neuromonitoring stehen dem Chirurg mehrere Möglichkeiten zu Verfügung, um sicherzugehen, dass keine kritischen Strukturen während der Operation verletzt werden. Insbesondere Faserverbindungen, welche für die grundlegenden menschlichen Funktionen wie Sprache, Sehen und Bewegung notwendig sind, werden mit einem hohen Aufwand vor ungewollten Beschädigungen während der Tumoroperation geschützt.
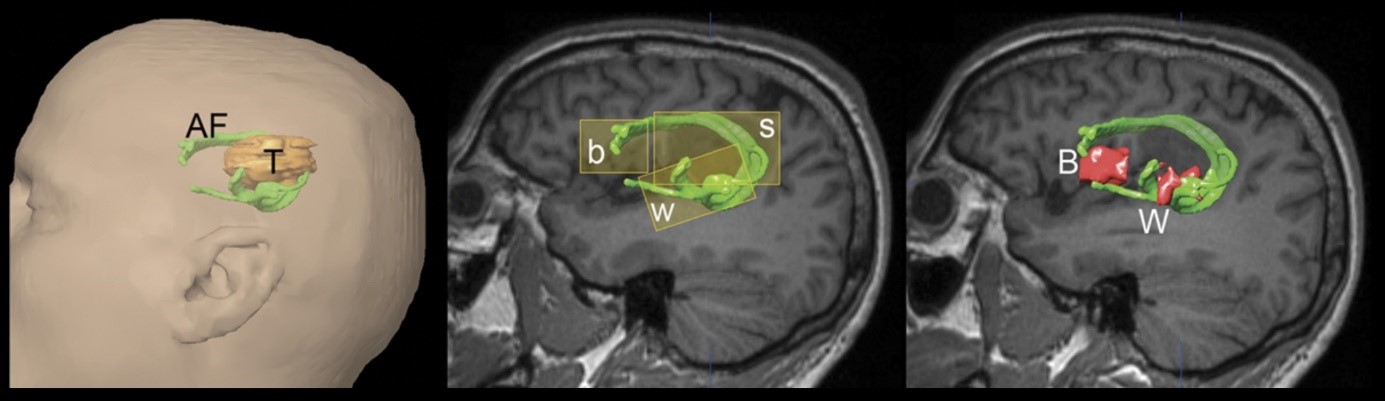
Tumorchirurgie. (Links) Der zu entfernende Tumor (T) liegt in unmittelbarer Nähe zum Fasciculus arcuatus (AF). Das mittlere Bild zeigt die sogenannten Voxels of Interest (VOI), welche zur Berechnung des Faserbündels herangezogen wurden. Rechts zeigt sich der Verlauf des Fasciculus arcuatus mit dem Broca-Zentrum (B) und dem Wernicke-Areal (W) am jeweiligen Ende des Faserbündels. Bild: Stieglitz et. al. 2012, Neurosurgery 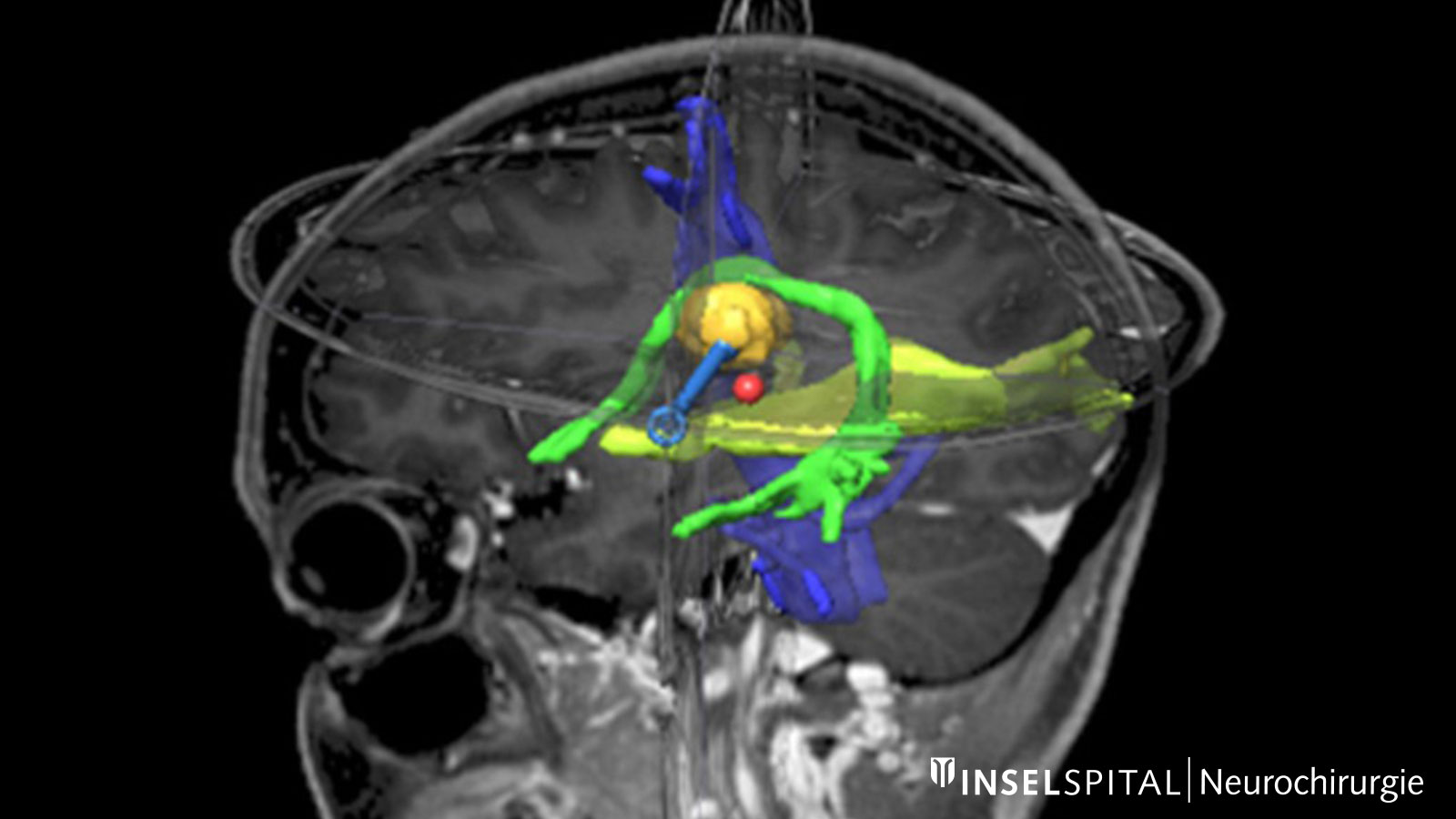
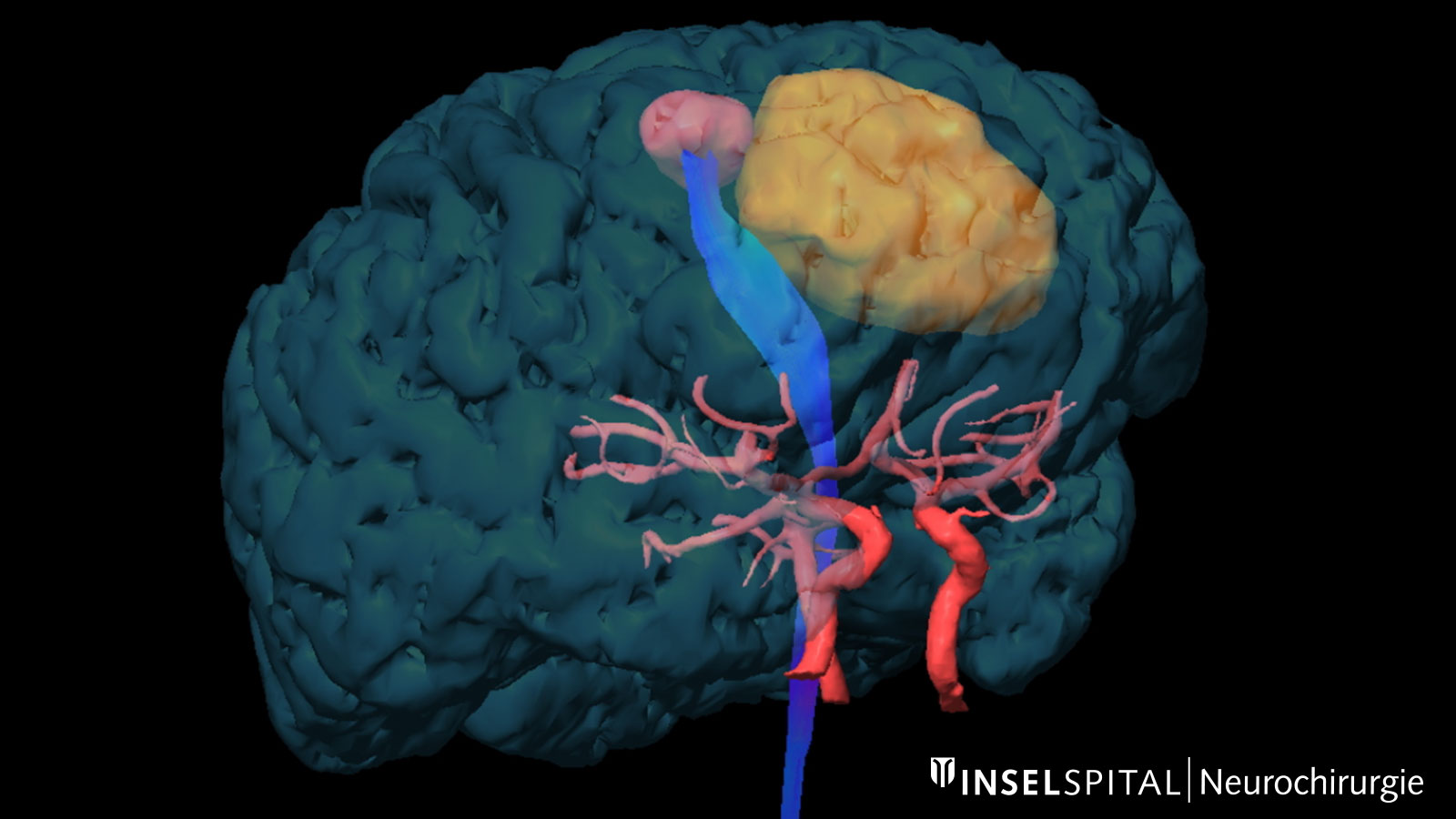
Eloquente Areale. Diese Abbildung zeigt einen Tumor (orange) inmitten funktionell wichtiger Areale: Tractus corticospinalis (blau), Tractus opticus (gelb) und Fasciculus arcuatus (grün) Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 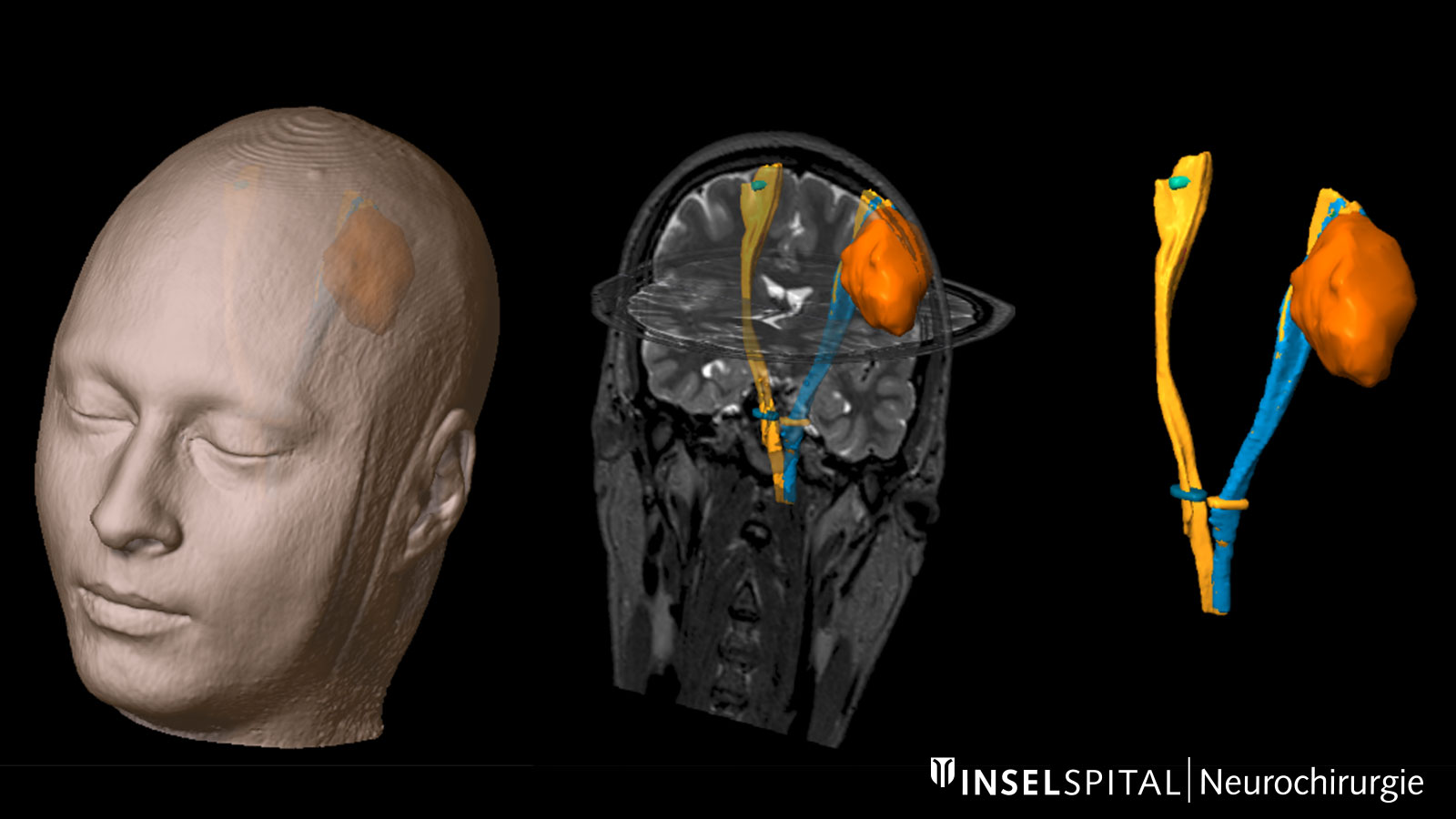
Kortikospinaler Trakt. Der kortikospinale Trakt (gelb und blau) ist hier als Faserbahn der motorischen Funktion in Relation zu einem Tumor (orange) dargestellt. Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 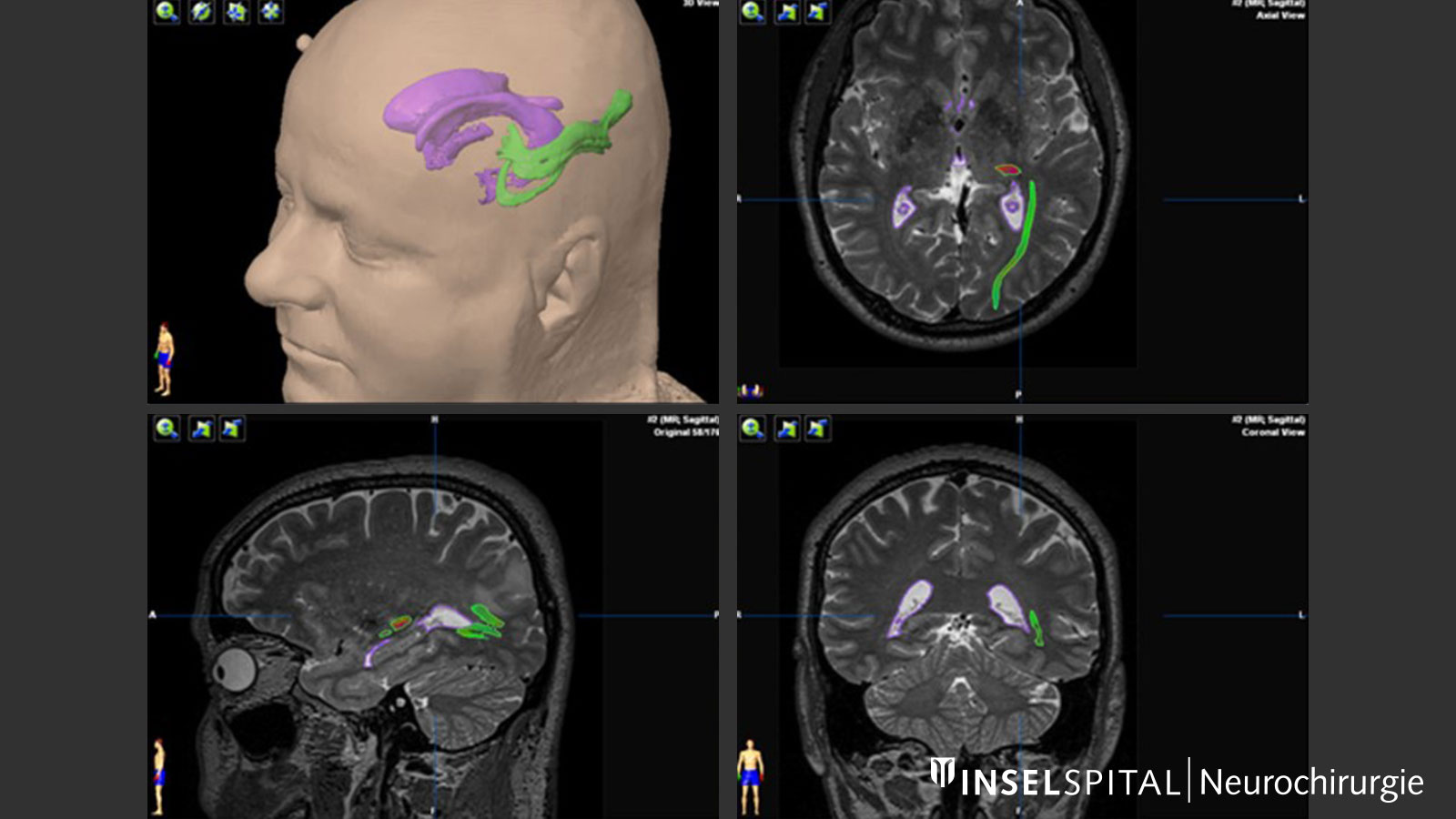
Sehbahn. Diese Abbildung verdeutlicht, wie die Sehbahn (tractus opticus, grün) um das Ventrikelsystem (lila) herum verläuft. Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 - Fiber Tracking bei der tiefen Hirnstimulation
Fiber Tracking beim essentiellen Tremor
Beim essentiellen Tremor verwenden wir das Fiber Tracking zur Visualisierung des dentatorubrothalamischen Trakts (DRTT) zur Planung einer Stimulation funktioneller Bahnen. Das Fiber Tracking ergänzt hier die herkömmliche, rein anatomische Planung. Der dentatorubrothalamische Trakt (DRTT) befindet sich im posterioren subthalamischen Areal (PSA) und ist einer der Zielpunkte bei der tiefen Hirnstimulation (kurz DBS von engl. deep brain stimulation) zur Behandlung von einem essentiellen Tremor *. Die exakte Lokalisierung ist unumgänglich bei der Operationsplanung, um eine präzise Stimulation des Trakts zu ermöglichen. Mittels Fiber Tracking können der Trakt bildlich dargestellt und die Zielpunkte für die DBS-Elektrodenimplantation optimal ermittelt werden.

Tiefe Hirnstimulation bei Tremorerkrankung. Das linke Bild zeigt die Visualisierung des dentatorubrothalamischen Trakts zur Planung der korrekten Elektrodenimplantation (rot) bei einer tiefen Hirnstimulation. Das rechte Bild zeigt die exakte Ziellokalisation, damit die Stimulation direkt neben dem DRTT stattfinden kann. Bild: Universitätsklinik für Neurochirurgie, Inselspital Bern © CC BY-NC 4.0 Fiber Tracking bei Depression
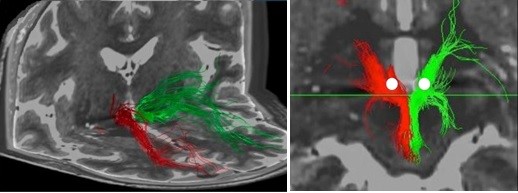
Tiefe Hirnstimulation bei Depressionen. Auf dem linken Bild ist eine 3D-Rekonstruktion des rechten (rot) und linken (grün) medialen Vorderhirnbündels dargestellt. Auf dem rechten Bild sind die Zielpunkte für die Elektrodenplatzierung vor der Tiefen Hirnstimulation als weisse Punkte markiert. Bild: Fenoy et. al. 2016, J Affect Disord Ein weiterer klinischer Anwendungsbereich für das Fiber Tracking am Inselspital stellt die Therapie mittels tiefer Hirnstimulation (kurz DBS von engl. deep brain stimulation) bei schweren Fällen von Depression dar, die auf die übliche Therapie nicht ansprechen. Es wurde in medizinischen Studien gezeigt, dass die Stimulation des superolateralen Anteils des medialen Vorderhirnbündels einen positiven Therapieeffekt bei refraktären Depressionen hat *. Um das Faserbündel korrekt zu identifizieren und die Zielkoordinaten für die DBS festzulegen, ist im Vorfeld des Eingriffs ein Fiber Tracking notwendig.
Referenzen
-
Nowacki A, Debove I, Rossi F, Schlaeppi J, Petermann K, Wiest R, Schüpbach M, Pollo C. Targeting the posterior subthalamic area for essential tremor: proposal for MRI-based anatomical landmarks. Journal of Neurosurgery. 2018;1-8.
-
Fenoy AJ, Schulz P, Selvaraj S, Burrows C, Spiker D, Cao B, et. al. Deep brain stimulation of the medial forebrain bundle: Distinctive responses in resistant depression. J Affect Disord. Oktober 2016;203:143–51.
